
发布日期:2026-04-17浏览次数:175来源:蓝景科信

文献题目:The PtobZIP55–PtoMYB170 module regulates the wood anatomical and chemical properties of Populus tomentosa in acclimation to low nitrogen availability
发表期刊:Journal of Integrative Plant Biology
影响因子:9.3
发表时间:2024.11.14
发表单位:中国林业科学研究院林业研究所
蓝景科信提供:DAP-seq技术服务
主要研究内容
木材(次生木质部)是建筑、造纸和生物能源的重要原料,其形成是受多种转录因子和环境因素协同调控的复杂生物学过程。毛白杨是我国重要的速生用材树种,但其人工林多建于氮素贫瘠土壤,低氮胁迫严重制约其生长和木材形成。现有研究已证实bZIP和MYB类转录因子参与木材发育调控,但其在低氮条件下调控木质部形成的分子机制尚不明确。
PtobZIP55作为S1-bZIP亚家族核定位转录因子,在毛白杨次生木质部中特异性高表达且受低氮显著诱导。功能验证表明,过表达PtobZIP55可缓解低氮造成的生长抑制与叶片黄化,优化木材解剖结构并促进木质素沉积;敲除则表现相反的表型,且该调控仅作用于木质素、不影响纤维素含量。进一步分子实验证实,PtobZIP55可直接结合PtoMYB170启动子的G-box元件并激活其转录,二者表达模式与功能高度协同。
研究借助DAP-seq技术共鉴定出431个PtoMYB170 潜在靶基因,明确其的核心结合基序为典型AC元件,并从中筛选出木质素合成关键基因PtoDAHPS1、PtoEMB1144、PtoPAL1、PtoCSE1。后续通过酵母单杂交、ChIP-qPCR及双荧光素酶实验证实,PtoMYB170 可直接结合并转录激活上述4个木质素合成关键基因,且这些靶基因均受低氮诱导表达。同时,PtoMYB170还能调控苯丙氨酸解氨酶(PAL)的表达与酶活,通过PAL介导的氮素循环途径提升氮素利用效率,最终完整构建“PtobZIP55-PtoMYB170-木质素合成基因”的低氮适应调控通路。
本研究系统解析了杨树响应低氮胁迫的木材形成调控机制,为培育耐贫瘠、木材品质优良的杨树新品种提供了理论依据与关键基因靶点。
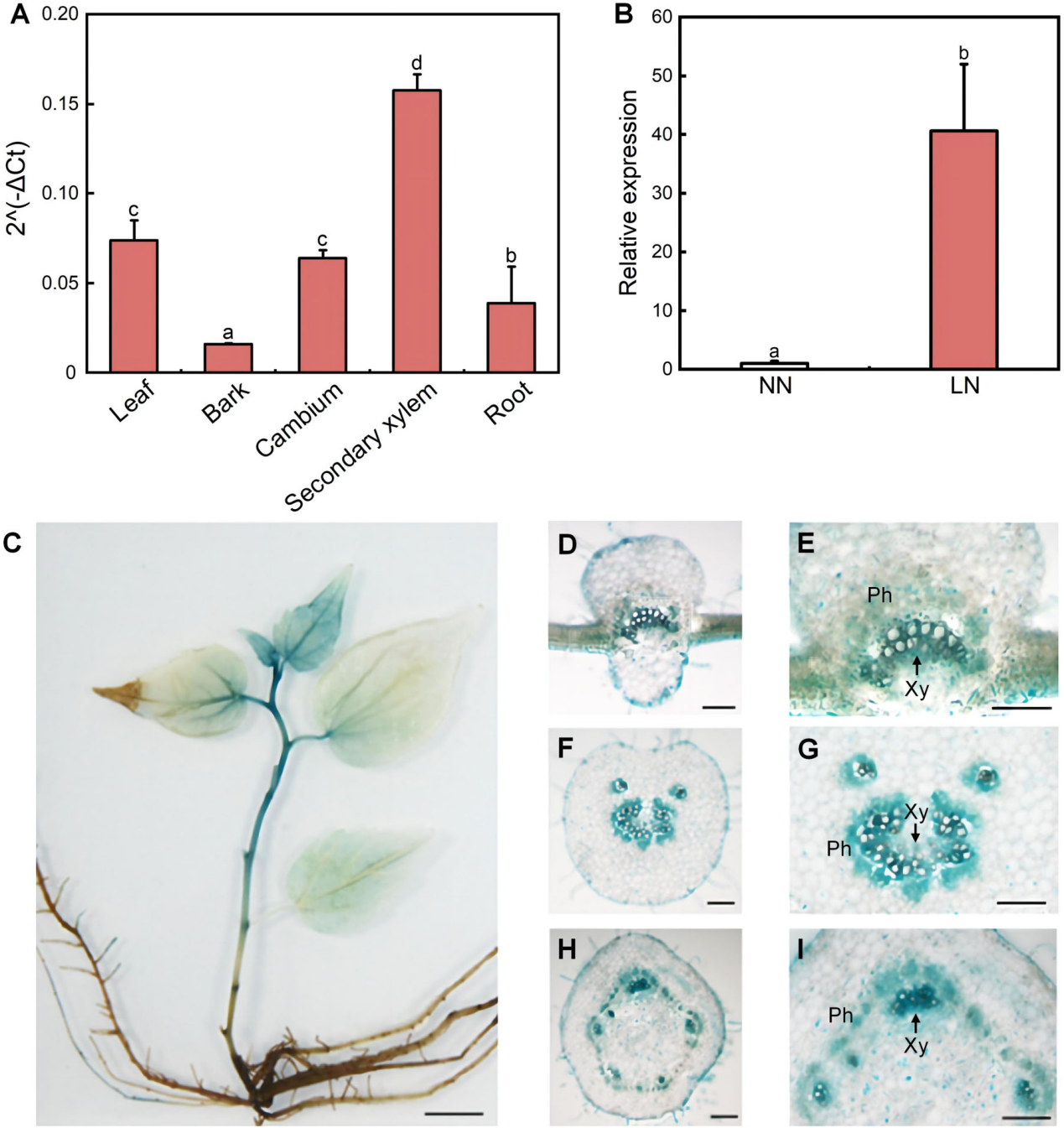
图1. PtobZIP55基因的表达模式。(A)PtobZIP55基因在毛白杨不同组织中的表达模式。(B)正常氮(NN)和低氮(LN)条件下,PtobZIP55基因在次生木质部中的相对表达量。图A和图B中的柱形图数值为平均值±标准误(n=3),各子图中柱形图上不同字母表示处理间存在显著差异。(C~I)在PtobZIP55启动子驱动GUS报告基因的转基因植株中,检测到GUS基因在幼苗(C)及多种维管组织中的表达,包括叶脉(D、E)、叶柄(F、G)和茎(H、I)。Xy代表木质部,Ph代表韧皮部。比例尺:C为1 cm,D~I为100 μm。
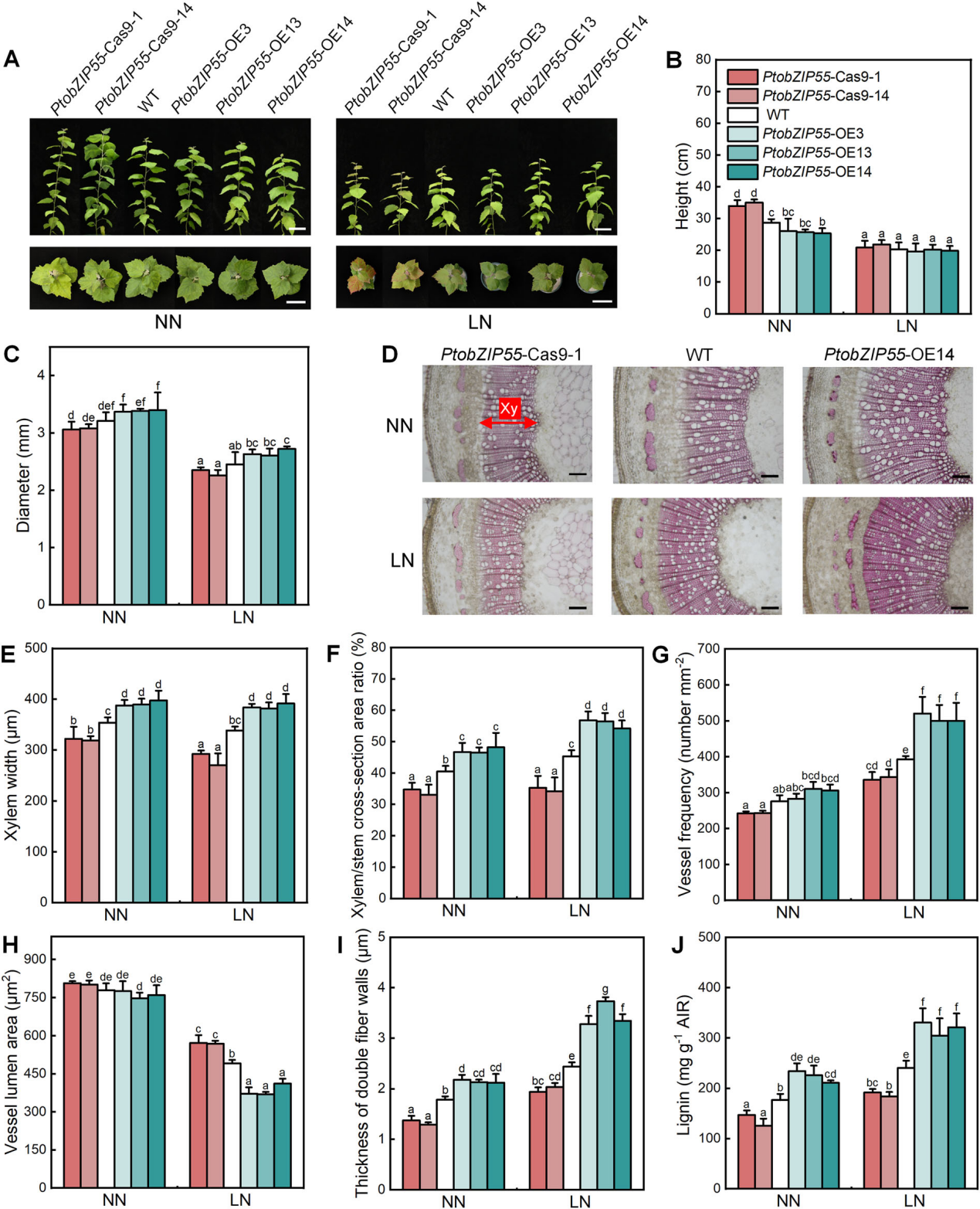
图2. 正常氮(NN)和低氮(LN)条件下培养2个月的4月龄毛白杨PtobZIP55敲除株系、过表达株系及野生型(WT)植株的形态特征与木材性状。(A)NN和LN条件下PtobZIP55转基因植株与野生型植株的生长表现,比例尺为10 cm。(B、C)PtobZIP55转基因植株与野生型植株的株高(B)和茎粗(C)。(D)经盐酸-间苯三酚染色的PtobZIP55转基因植株与野生型植株茎第八节间横切片,Xy代表木质部,比例尺为100 μm。(E~I)PtobZIP55转基因植株与野生型植株茎的木质部宽度(E)、木质部/茎横截面积比(F)、导管频率(G)、导管管腔面积(H)及双纤维细胞壁厚度(I)。(J)PtobZIP55转基因植株与野生型植株次生木质部中的木质素含量。图(B、C)及(E~J)中柱形图数值为平均值±标准误(n=3),各子图中柱形图上不同字母表示组间存在显著差异(P<0.05)。
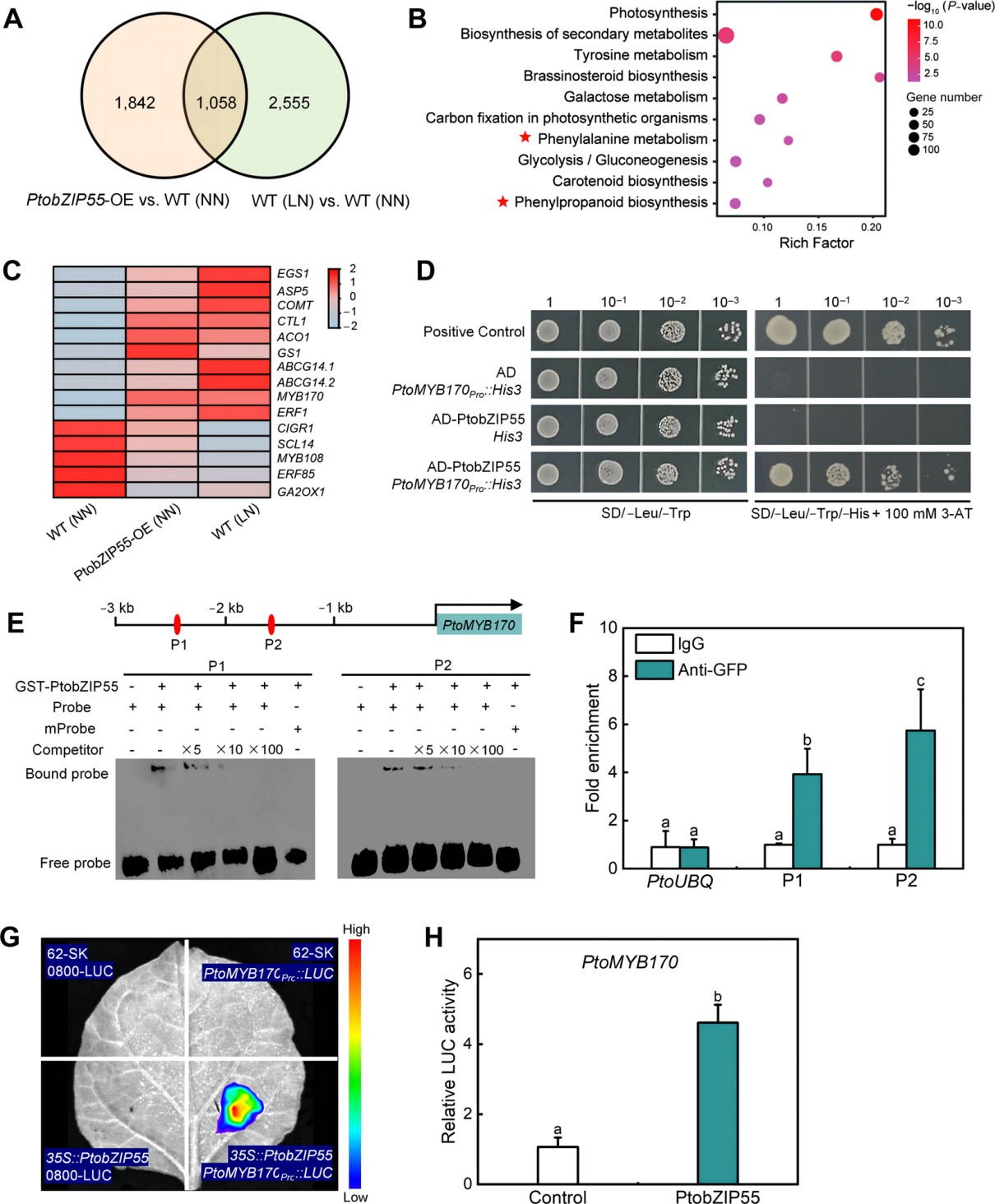
图3. PtobZIP55调控靶基因的转录组分析及PtobZIP55直接结合PtoMYB170启动子序列并激活其表达(A)韦恩图展示正常氮(NN)条件下PtobZIP55过表达株系与野生型(WT)杨树的差异显著表达基因(SDEGs)数量,以及低氮(LN)与正常氮处理的野生型杨树间的差异显著表达基因数量。(B)对PtobZIP55 过表达株系与正常氮野生型、低氮与正常氮处理野生型这两组对比中共同的差异显著表达基因进行KEGG通路分析。(C)与正常氮供应的野生型杨树相比,两组对比中共同参与木质素生物合成且呈同步上调或下调的差异显著表达基因的表达水平。(D)酵母单杂交实验验证,酵母细胞中PtobZIP55可与PtoMYB170的启动子序列相结合。(E)EMSA实验证实,体外条件下PtobZIP55可结合PtoMYB170启动子区域的两个位点(P1和P2)。(F)ChIP-qPCR实验表明,体内条件下PtobZIP55可结合PtoMYB170启动子区域的两个位点(P1和P2);以PtobZIP55-绿色荧光蛋白(GFP)融合蛋白表达植株的染色质为材料,用抗GFP抗体进行免疫沉淀,以免疫球蛋白G(IgG)作为阴性对照,毛白杨泛素基因(PtoUBQ)作为内参基因。(G)本氏烟草叶片中PtobZIP55激活PtoMYB170启动子的双荧光素酶报告基因实验。实验组为35S::PtobZIP55+PtoMYB170Pro::LUC,阴性对照组为62-SK+0800-LUC、35S::PtobZIP55+0800-LUC和62-SK+PtoMYB170Pro::LUC。侵染后第3天记录荧光图像。(H)检测LUC和REN酶活性,计算二者活性比值作为最终的转录活性。以62-SK+PtoMYB170Pro::LUC作为对照,其LUC/REN比值设定为1。图(F)、(H)中柱形图数值为平均值±标准误(n=3),各子图中柱形图上不同字母表示实验组与对照组间存在显著差异。
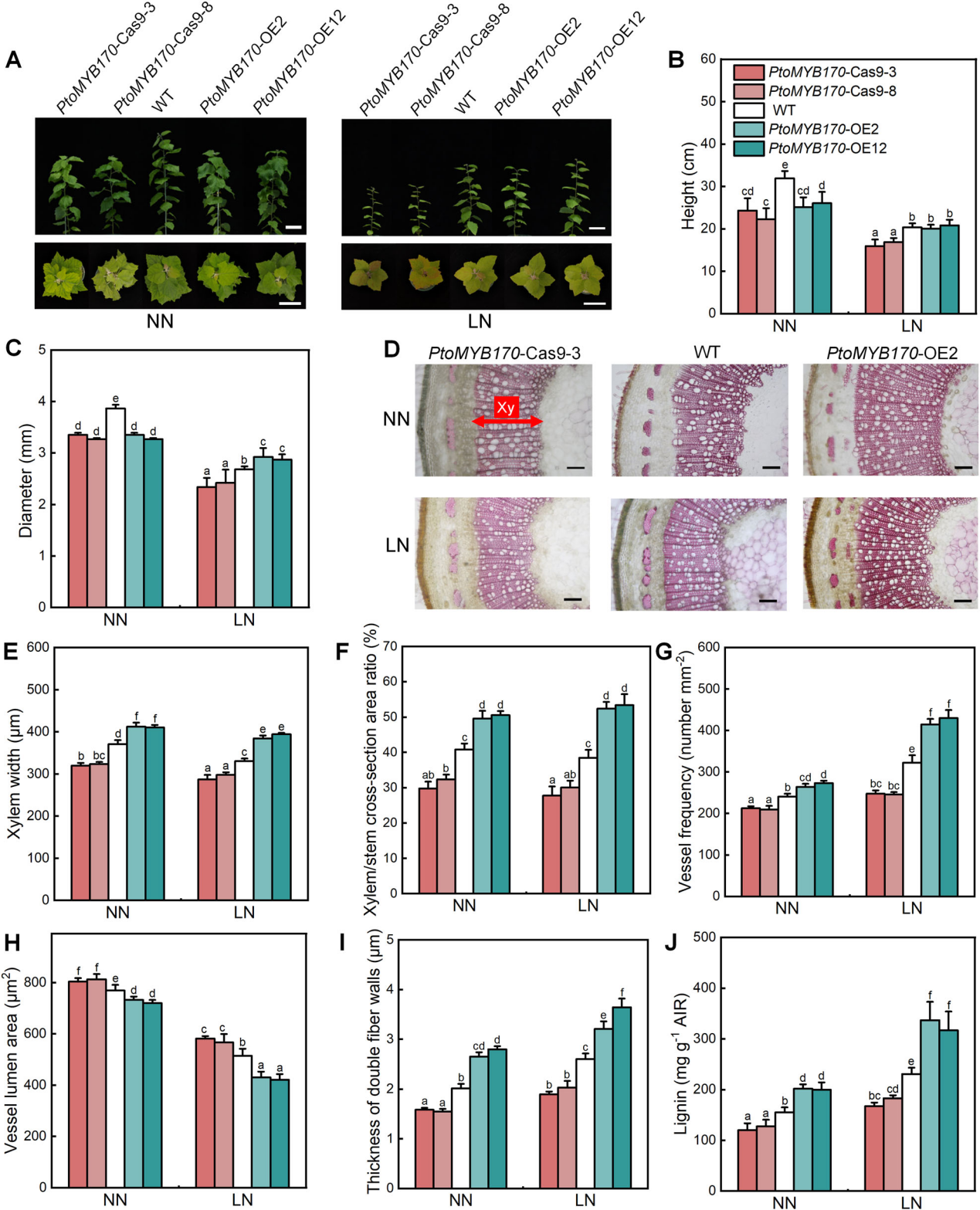
图4. 正常氮(NN)和低氮(LN)条件下培养2个月的4月龄毛白杨PtoMYB170 敲除株系、过表达株系及野生型(WT)植株的形态特征与木材性状。(A)PtoMYB170转基因及野生型杨树的生长表现。比例尺为10 cm。(B、C)PtoMYB170转基因及野生型杨树的株高(B)和茎粗(C)。(D)经盐酸-间苯三酚染色的PtoMYB170转基因及野生型杨树茎第八节间横切片。Xy为木质部。比例尺为100μm。(E~I)PtoMYB170转基因及野生型杨树茎的木质部宽度(E)、木质部/茎横截面积比(F)、导管频率(G)、导管管腔面积(H)及双纤维细胞壁厚度(I)。(J)PtoMYB170转基因及野生型杨树次生木质部中的木质素含量。图(B、C)及(E~J)中柱形图数值为平均值±标准误(n=3),各子图中柱形图上不同字母表示组间存在显著差异(P<0.05)。
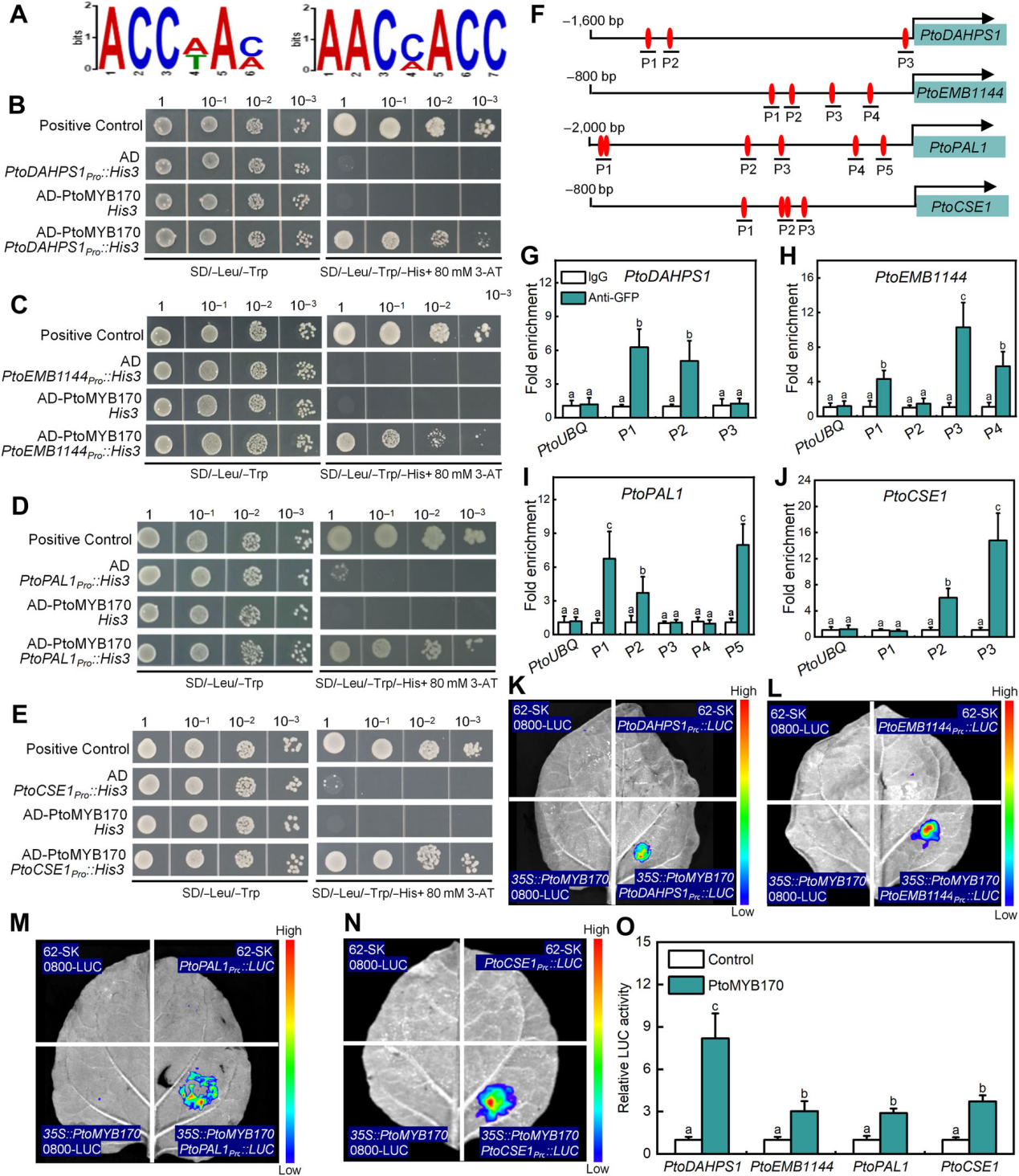
图5. PtoMYB170直接结合PtoDAHPS1、PtoEMB1144、PtoPAL1 和 PtoCSE1 的启动子序列。(A)通过DAP-seq鉴定得到的PtoMYB170靶基因的潜在结合元件。(B~E)酵母单杂交实验验证,酵母细胞中PtoMYB170可分别结合PtoDAHPS1(B)、PtoEMB1144(C)、PtoPAL1(D)和PtoCSE1(E)的启动子序列。(F)PtoMYB170在PtoDAHPS1、PtoEMB1144、PtoCSE1和PtoPAL1启动子序列上的结合位点示意图。(G~J)ChIP-qPCR实验证实,体内条件下PtoMYB170可结合上述靶基因的启动子序列;以PtoMYB170-绿色荧光蛋白(GFP)融合蛋白表达植株的染色质为材料,采用抗GFP抗体进行免疫沉淀,以免疫球蛋白G(IgG)作为阴性对照,毛白杨泛素基因(PtoUBQ)作为内参基因。(K~N)本氏烟草叶片中PtoMYB170激活各靶基因启动子的双荧光素酶报告基因实验;以35S启动子驱动的PtoMYB170表达载体与各靶基因启动子驱动的荧光素酶(LUC)报告载体共转化组为实验组,以62-SK空载体与0800-LUC空载体共转化组、35S::PtoMYB17与0800-LUC共转化组、62-SK与各靶基因启动子驱动的LUC报告载体共转化组为阴性对照,侵染后第3天记录荧光图像。(O)检测LUC和REN的酶活性,计算二者活性比值作为最终的转录活性。以62-SK空载体与各靶基因启动子驱动的LUC报告载体共转化组为对照,并将各对照组的LUC/REN比值均设为1。图(G~J)、(O)中柱形图数值为平均值±标准误(n=3),各子图中柱形图上不同字母表示实验组与对照组间存在显著差异。
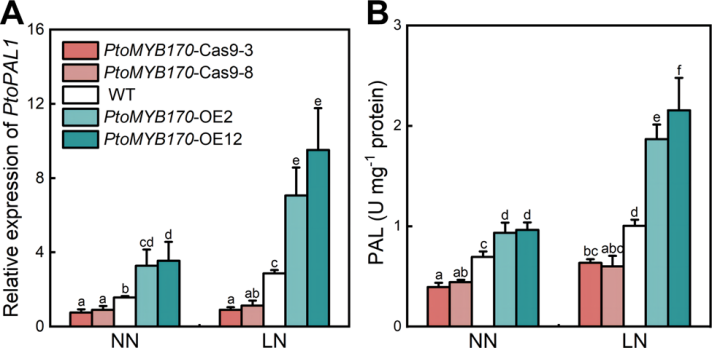
图6. 正常氮(NN)和低氮(LN)条件下,毛白杨PtoMYB170敲除株系、过表达株系及野生型(WT)植株次生木质部中PtoPAL1基因的表达水平及其酶活性。(A、B)分别为PtoMYB170转基因株系及野生型植株中PtoPAL1基因的表达水平(A)和苯丙氨酸解氨酶(PAL)的酶活性(B)。各子图中柱形图数值均为平均值±标准误(n=3),柱形上方不同字母表示组间存在显著差异(P<0.05)。
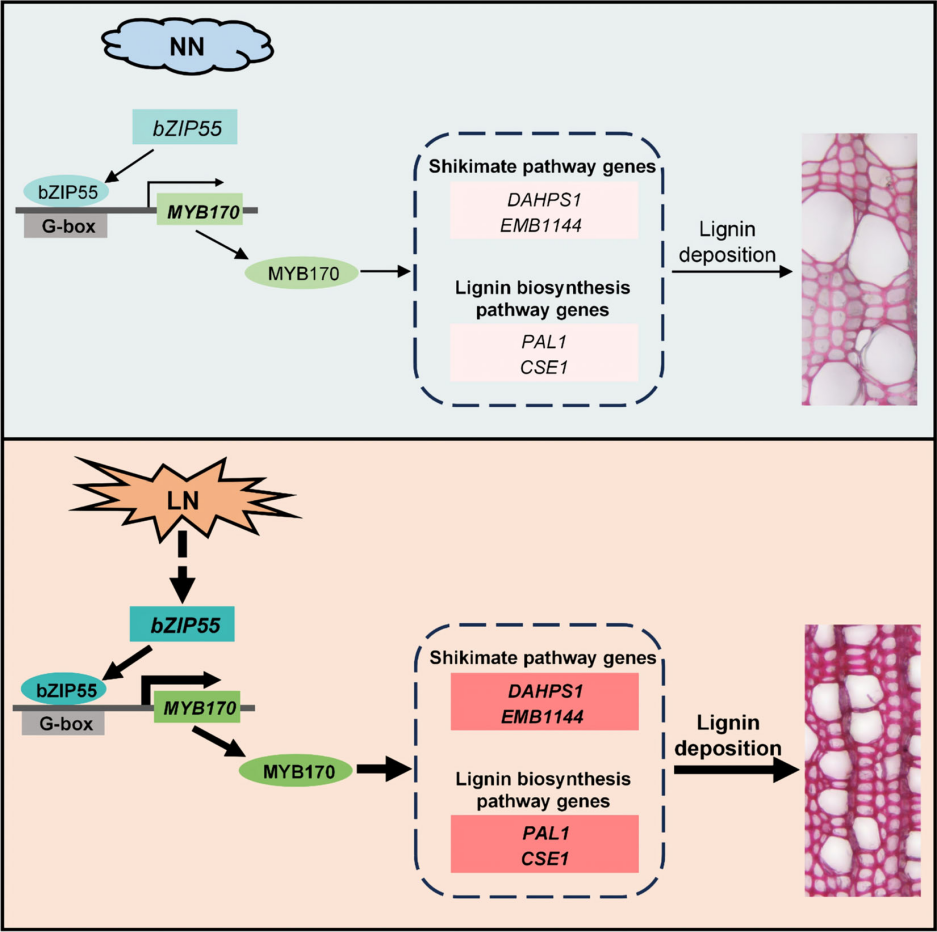
图7. 毛白杨适应低氮(LN)条件下,PtobZIP55激活PtoMYB170转录并进一步正向调控木质素生物合成基因、促进次生木质部木质素沉积的调控模式示意图。低氮诱导PtobZIP55的转录水平上调,PtobZIP55结合到PtoMYB170的启动子序列并激活其表达;PtoMYB170进一步结合到木质素生物合成通路关键基因PtoDAHPS1、PtoEMB1144、PtoPAL1和PtoCSE1的启动子序列,提高这些基因的转录水平,最终导致毛白杨次生木质部中木质素含量增加。基因表达水平与木质素浓度随低氮环境变化呈增强趋势,该过程通过箭头及深色背景加粗文本框进行标注。
